
起業理念
私達はMSCが本来持つはずの細胞機能である増殖能と分化能と細胞の均一性や遊走能を活かした安全かつ効果的な幹細胞治療に結びつけることを目指しています。
間葉系幹細胞治療の現状と問題点
間葉系幹細胞は細胞採取に伴う倫理的問題が少なく、骨・軟骨・脂肪などへの多様な分化能を持つことから、造血幹細胞に次いで臨床応用が期待されている組織幹細胞で、比較的簡単な手技により分離できることから、主に試験管内で軟骨・骨などへ分化誘導後に局所へ移植するなど、バイオマテリアルの材料として広く用いられており、国内でも島根大学をはじめとするいくつかの臨床施設にて医師主導型臨床治験が開始されている。また米国では300件以上の臨床試験が行われている。
現在流通している間葉系幹細胞は、骨髄単核細胞を培養皿上に播種し、2~3週間培養後に出現する繊維芽細胞様のコロニー形成細胞(CFU-F)を回収するという方法で得るが、この手法で得た付着細胞集団は分化能を持たない夾雑細胞の混入が避けられないために、細胞品質を一定に保つことが困難である上に、培養中に骨髄内にいる時には備えていた遊走性、すなわち体内を循環する能力を失っているために投与方法が限定される、など様々な問題を含んでいる。
PuRECではその細胞が本来持つ細胞機能を失わせずに細胞を分離する手順を確立しており、この手法で得た品質の良い間葉系幹細胞を基礎・臨床研究用途に提供することを目的として設立されます。
増殖性:未分化性を失わずに自己増幅する機能
分化能:多種多用な細胞に変化することのできる機能
遊走性:体内を循環し適切な場所へ移動し生着する機能
用途:骨疾患・免疫疾患・慢性的な炎症性疾患など、治療の難しい疾患を治癒に導く作用
移植方法:従来型の局所移入だけでなく全身性移入が可能
これらの条件を全てそなえています

フローサイトメトリーと選択的マーカーを用いた細胞分離方法によって超高純度なヒト間葉系幹細胞を得ることが可能になりました
超高純度間葉系幹細胞
REC: Rapidly Expanding Cells
研究責任者の松崎らは文部科学省・再生医療の実現化プロジェクトを通じてLNGFR (CD271) Thy1 (CD90)の2種の抗体を用いることで極めて効率よくヒトMSCを選別することができることを明らかにし、骨髄・末梢血・胎盤絨毛膜・歯髄からセルソータを用いて超高純度なヒト間葉系幹細胞(REC)を分離する技術を開発した。
RECは従来方で分離した間葉系幹細胞と比較し、A) 均一な細胞集団である、B)細胞老化を示していない、C) 細胞の大部分が増殖期にある、D) 高い分化能(特に脂肪分化能)を示す、E) 遊走性を示すなど、これまで問題となっている点をすべてクリアした高品質かつ高純度なヒトMSCと言える (Mabuchi et al. Stem Cell Reports 2013)
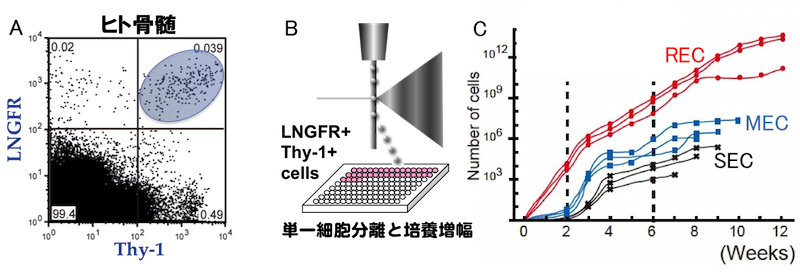

通常方法で得た間葉系幹細胞とは異なり、RECは一切の夾雑細胞を含まず、長期間の培養増幅が可能です。また一定期間の培養後も分化・遊走能が維持されています。さらに凍結細胞として保存が可能で、いつでも研究に用いることができます。つまり基礎研究用細胞として、あるいは臨床研究用細胞として、細胞品質が保証された間葉系幹細胞を利用することができます。
間葉系幹細胞(MSC)の機能と治療効果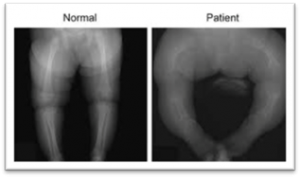
治療法がない、生まれつきの骨や軟骨をうまく作ることができない病気に対して、MSC移植は有効な治療となることが期待されています
- 骨・軟骨・脂肪の再生
骨軟骨形成不全・乳房再建など - 免疫調節
GVHD・クローン病・多発性硬化症など - 傷を治す
脳卒中・心筋梗塞・肝硬変など
予定されている製品

高純度な間葉系幹細胞
PuRECが独自に開発した細胞分離技術を用いて精製した高純度の間葉系幹細胞を凍結バイアルに封入し、研究用途の間葉系幹細胞製品として販売します。
高純度間葉系幹細胞の分離受託サービス
移植医療への適合を視野に入れ、細胞性能が保証され、GMPに準拠したレベルの高純度な幹細胞を安定的に提供する体制を整備し、臨床用高純度MSC分離システムを構築し、臨床施設への細胞分離・培養受託サービスを提供します。
間葉系幹細胞分離用・評価用試薬
高純度間葉系幹細胞に特化した染色性を示すモノクローナル抗体をナノ磁気微粒子と結合させることによって、間葉系幹細胞分離用試薬として提供します。また分離した間葉系幹細胞の品質を検定するための細胞評価用の試薬として、蛍光物質結合抗体、細胞染色用試薬を提供します。
細胞培養用試薬
間葉系幹細胞を医療へ応用する際、自己増殖能と分化能を有するには安定的な培養環境が必要となるため、培養増幅に最適化された培養用試薬を提供します。
間葉系幹細胞移植医療は、すでに臨床応用はされているものの、既存の手法で分離された細胞は幹細胞としてはわずか0.1-1%が含まれているにすぎず、純度に課題が残る。再生医療の市場は「間葉系幹細胞関連の国内再生医療市場予測((株)矢野経済研究所:2004 年度)」によると、2010 年に112,000 件、2015 年に218,720 件と予想されている。今後、先進諸国の高齢化が進むとともに、さらに患者数が増え続けるものと考えられる。また、米国では再生医療関連の市場は2020 年には6,000億円に成長すると推定されており、高純度間葉系幹細胞を用いた再生医療への社会的貢献、社会経済への効果は大きいものと予想される。
ヒトMSCはLonza社やStem Cell Technology社など海外企業数社より販売されているが、そのほぼ全てが既存の骨髄単核細胞を培養し2週間後に回収した従来通りの細胞集団である。このため、商用的に流通している培養MSCはロットによって分化能や増殖能に大きな差が見られ、バイオマテリアル等の材料として、あるいは臨床応用に供する上で再現性即ち安全性を確保することが困難であることが大きな問題となっている。
RECと他社市販細胞を比較したところ、いずれのメーカーの細胞においても、細胞増殖の速さや分化能に違いが認められた。従って高品質な製品を安定して供給できれば、現在凍結MSCを利用している研究者や企業に広く利用されると予想できる。

Our goal
is to harness the inherent cell functions of MSCs, such as proliferation, differentiation, uniformity, and migration, to develop safe and effective stem cell therapies.
Current Status and Issues in Mesenchymal Stem Cell Therapy
Mesenchymal stem cells (MSCs) are tissue stem cells that are expected to be the next most clinically applicable after hematopoietic stem cells because of their diverse differentiation potential, including bone, cartilage, and fat, and because they can be isolated using relatively simple procedures. Because they can be differentiated in vitro into cartilage and bone, followed by local transplantation, they are widely used as biomaterials. Investigator-initiated clinical trials have begun at several clinical facilities in Japan, including Shimane University. More than 300 clinical trials are also underway in the United States.
Currently available mesenchymal stem cells are obtained by seeding bone marrow mononuclear cells onto culture dishes and recovering fibroblast-like colony-forming cells (CFU-Fs) that emerge after 2–3 weeks of culture. However, the adherent cell population obtained using this method inevitably contains contaminating cells that lack differentiation potential, making it difficult to maintain consistent cell quality. Furthermore, they lose the migratory ability (i.e., the ability to circulate throughout the body) that they possess while in the bone marrow during culture, limiting the method of administration. These issues present several challenges.
PuREC has established a procedure for isolating cells without losing their inherent cellular functions, and will be established with the aim of providing high-quality mesenchymal stem cells obtained using this method for basic and clinical research purposes.
Proliferation: The ability to self-multiply without losing their undifferentiated state Differentiation: The ability to transform into a wide variety of cells Migratory: The ability to circulate within the body, migrate to appropriate locations, and engraft Uses: Leads to the cure of difficult-to-treat diseases such as bone diseases, immune disorders, and chronic inflammatory diseases Transplantation method: Systemic transplantation is possible in addition to conventional local transplantation All of these conditions are met.

It is now possible to obtain ultra-pure human mesenchymal stem cells using a cell separation method using flow cytometry and selective markers.
Ultra-Pure Mesenchymal Stem Cells
(REC: Rapidly Expanding Cells)
Research Director Matsuzaki et al., through the Ministry of Education, Culture, Sports, Science and Technology (MEXT) Regenerative Medicine Realization Project, demonstrated that human MSCs can be efficiently selected using two antibodies, LNGFR (CD271) and Thy1 (CD90), and developed a technology to isolate ultra-pure human mesenchymal stem cells (RECs) from bone marrow, peripheral blood, placental chorion, and dental pulp using a cell sorter.
Compared to mesenchymal stem cells isolated by conventional methods, RECs are characterized by: A) homogeneous cell populations; B) no cellular senescence; C) the majority of cells are in the proliferation phase; D) high differentiation potential (especially adipogenic potential); and E) migratory potential. These characteristics make them high-quality, highly purified human MSCs, overcoming all of the previously troubling issues (Mabuchi et al. Stem Cell Reports 2013).
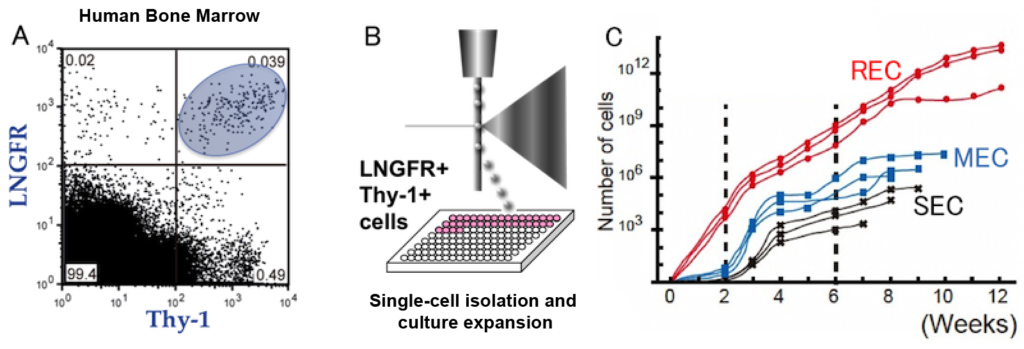

Unlike mesenchymal stem cells obtained using conventional methods, RECs contain no contaminating cells and can be cultured and expanded for long periods of time. They also maintain their differentiation and migration capabilities even after a certain period of culture. Furthermore, they can be stored as frozen cells and used for research at any time. This means that mesenchymal stem cells with guaranteed cell quality can be used for basic research or clinical research.
Functions and therapeutic effects of mesenchymal stem cells (MSCs)
MSC transplantation is expected to be an effective treatment for diseases for which there is no cure and in which the body is unable to properly produce bone and cartilage.
- Bone, cartilage, and fat regeneration
, osteochondrodysplasia, breast reconstruction, etc. - Immunomodulation
GVHD, Crohn’s disease, multiple sclerosis, etc. - Healing wounds
Stroke, myocardial infarction, cirrhosis of the liver, etc.
Planned products


Highly purified mesenchymal stem cells
are purified using PuREC’s proprietary cell separation technology and sealed in cryovials for sale as mesenchymal stem cell products for research use.
High-purity mesenchymal stem cell isolation service:
offer reagents for isolating mesenchymal stem cells by conjugating monoclonal antibodies that specifically stain highly purified mesenchymal stem cells with nanomagnetic particles. We also offer fluorescent-conjugated antibodies and cell staining reagents as cell evaluation reagents for assessing the quality of isolated mesenchymal stem cells.
Reagents for Isolation and Evaluation of Mesenchymal Stem Cells We
offer reagents for isolating mesenchymal stem cells by conjugating monoclonal antibodies that specifically stain highly purified mesenchymal stem cells with nanomagnetic particles. We also offer fluorescent-conjugated antibodies and cell staining reagents as cell evaluation reagents for assessing the quality of isolated mesenchymal stem cells.
Cell Culture Reagents
For mesenchymal stem cells (MSCs) to be used in medical applications, a stable culture environment is required to maintain their self-proliferation and differentiation capabilities. We offer culture reagents optimized for expansion. While
mesenchymal stem cell transplantation has already been clinically applied, purity remains an issue, with cells isolated using existing methods only containing 0.1-1% stem cells. According to the “Domestic Mesenchymal Stem Cell-Related Regenerative Medicine Market Forecast (Yano Research Institute, Ltd.: 2004),” the regenerative medicine market is expected to reach 112,000 cases in 2010 and 218,720 cases in 2015. As developed countries experience aging, the number of patients is expected to continue to increase. Furthermore, the regenerative medicine market in the United States is estimated to grow to 600 billion yen by 2020, and the social and economic impact of regenerative medicine using highly purified MSCs is expected to be significant.
Human MSCs are commercially available from several overseas companies, including Lonza and Stem Cell Technology. However, almost all of these products are conventional cell populations, harvested after two weeks of culturing existing bone marrow mononuclear cells. As a result, commercially available cultured MSCs exhibit significant variations in their differentiation and proliferation potential depending on the lot. This poses a major problem for ensuring reproducibility, i.e., safety, when used as biomaterials or for clinical applications.
When comparing REC with commercially available cells from other companies, differences were observed in the rate of cell proliferation and differentiation potential between the two manufacturers. Therefore, if a stable supply of high-quality products can be achieved, it is expected that these products will be widely used by researchers and companies currently using frozen MSCs.
